Aproveitando a minha passagem pela RM Neuro, no dia
17/10/2012, surgiu um caso de uma patologia rara, hereditária chamada
Adrenomieloneuropatia. Assim, decidi escolher este tema a abordar.
“Adrenomieloneuropatia (AMN) é uma
variante da adrenoleucodistrofia (ALD), doenças hereditárias raras ligadas ao
cromossoma X” (Khandwala, et. al., 2004). O termo de ALD foi sugerido primeiramente nos anos 70 e em 1976
foi reportado o primeiro caso de AMN (Assies, et. al., 1997).
“A Adrenoleucodistrofia (ALD) é uma doença
hereditária, ligada ao cromossoma X, do metabolismo peroxissomal,
bioquimicamente caracterizada pela acumulação de ácidos graxos de cadeia muito longa”. Este depósito provoca significativas alterações no sistema nervoso
central e periférico, ao nível da desmielinização, bem como o desenvolvimento
de uma insuficiência suprarrenal e hipogonadismo (Assies, et. al., 1997). “A frequência de X-ALD ou X-AMN nos
indivíduos do sexo masculino nos EUA é de 1:42 000” (Khandwala, et. al.,
2004).
Em termos gerais, a ALD manifesta-se numa idade mais
jovem, afectando sobretudo o cérebro enquanto que a AMN surge numa idade mais
avançada, envolvendo mais a medula espinhal, como irá ser comentado futuramente (Khandwala,
et. al., 2004).
PATOGENIA
Quer a ALD quer a
AMN são distúrbios dos peroxissomas, organelos intracelulares, que integram em
múltiplos mecanismos, um dos quais, o metabolismo dos ácidos graxos. Neste participam
especificamente, na oxidação de ácidos graxos de cadeia muito longa (VLCFAs) em
Acetil-CoA. Ora, os pacientes com uma destas patologias não produzem a enzima
Acetil-CoA sintetase, o que leva à acumulação de ácidos graxos de cadeia muito
longa. Como consequência, “há formação de
inclusões citoplasmáticas levando deste modo a uma disfunção progressiva do
sistema nervoso central, glândulas suprarrenais e testículos, uma vez que são
locais do metabolismo dos VLCFAs” (Khandwala, et. al., 2004).
“Nas variantes
cerebrais da ALD, é também visto uma resposta inflamatória, que será,
provavelmente a causa do dano da mielina observado. Patologicamente, estes
distúrbios caracterizam-se pela presença laminar de inclusões citoplasmáticas
constituídas por colesterol esterificado com VLCFAs” (Khandwala, et.
al., 2004).
 Ambas patologias,
ALD e AMN, como anteriormente referido, são transmitidas ligadas ao cromossoma
X. O gene localiza-se no braço longo do cromossoma X (Xq28), que codifica uma “proteína da membrana peroxissomal
pertencente à adenosina trifosfato da superfamília de proteínas
transportadoras”. Além disso, foram já identificados múltiplas formas de mutação
como deleções, mutações sem-sentido, deleções simples, entre outras (Khandwala,
et. al., 2004).
Ambas patologias,
ALD e AMN, como anteriormente referido, são transmitidas ligadas ao cromossoma
X. O gene localiza-se no braço longo do cromossoma X (Xq28), que codifica uma “proteína da membrana peroxissomal
pertencente à adenosina trifosfato da superfamília de proteínas
transportadoras”. Além disso, foram já identificados múltiplas formas de mutação
como deleções, mutações sem-sentido, deleções simples, entre outras (Khandwala,
et. al., 2004).
APRESENTAÇÃO CLÍNICA
“Vários
fenótipos podem ser distinguidos de acordo com a apresentação clínica e as suas
manifestações” (Kim & Kim, 2005), inclusive dentro de uma mesma família
podemos ter presente uma variabilidade fenotípica. Os dois fenótipos mais
frequentes são a ALD forma cerebral da infância e AMN com uma incidência de 45%
e 25% dos casos respectivamente (Khandwala, et. al., 2004).
Classicamente, podemos caracterizar a ALD forma
cerebral da infância por uma desmielinização cerebral rapidamente progressiva
levando a tetraparesia espástica, demência e uma disfunção visual e auditiva (Fauci
et al, Harrison, 17º edição).
Por outro lado, genericamente a AMN é considerada como
uma forma mais leve da ALD e também com uma progressão mais lenta. Os sintomas
neurológicos aparecem sobretudo, entre a 3ª e 4º década de vida.
Caracterizam-se sobretudo pelo “envolvimento
dos tratos ascendentes e descendentes longos da medula espinhal e pela
neuropatia periférica devido à desmielinização. Surge assim, parestesia
espástica e urinária bem como a disfunção eréctil” (Khandwala, et. al.,
2004).
 |
| 1º pico - ALD formas cerebrais Menores picos - AMN |
 |
| 1º curva - AMN 3º curva - ALD cerebral da infância |
 Cerca de “2/3 dos pacientes do sexo masculino têm uma
manifestação clínica ou subclínica de insuficiência suprarrenal e uma
significativa proporção tem associado uma disfunção gonadal (Fauci et al, Harrison, 17º edição).
Cerca de “2/3 dos pacientes do sexo masculino têm uma
manifestação clínica ou subclínica de insuficiência suprarrenal e uma
significativa proporção tem associado uma disfunção gonadal (Fauci et al, Harrison, 17º edição).
Aproximadamente cerca de 50% dos
heterozigóticos do sexo feminino apresentam sintomas neurológicos e 80% têm os
valores de VLCFAs elevados. Para além disso, os sintomas neurológicos surgem
mais tarde sendo mais leves, quando comparadas com os heterozigóticos masculinos.
Estes consistem sobretudo em leves sinais piramidais e incontinência urinária (Khandwala,
et. al., 2004).
DIAGNÓSTICO
O diagnóstico de ALD e AMN pode ser estabelecido
medindo os níveis absolutos dos VLCFAs. No entanto, é de realçar que “não há associação entre os níveis absolutos
VLCFAs e o grau de disfunção suprarrenal ou neurológica” (Khandwala, et.
al., 2004).
Assim, para avaliar o nível de insuficiência
suprarrenal e gonadal são pedidos (Fauci et al, Harrison, 17º edição):
· Níveis de cortisol
e ACTH;
· Teste de
estimulação de ACTH;
· Medição da
testosterona;
·
Medição dos níveis de gonadotrofinas
“A ressonância
magnética (RM) tornou-se essencial para avaliar quer o inicio do quadro clínico
quer a sua evolução. A RN permite assim detetar precocemente lesões no sistema
nervoso central e periférico” bem como distinguir os diferentes fenótipos
e com isso fazer o diagnóstico diferencial (Kim & Kim, 2005).
“Até
50% dos indivíduos do sexo masculino com AMN apresentam evidências radiológicas
da desmielinização cerebral na ressonância magnética (RM)” (Khandwala, et.
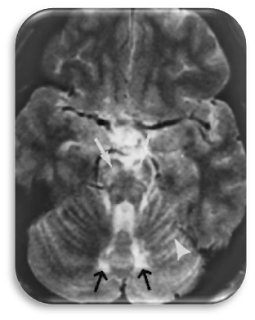
al., 2004). Podemos observar na RM:
1. Sem
achados cerebrais (55%) – AMN “Pura”: Atrofia da medula espinhal;
2. AMN
com envolvimento cerebral – Degeneração do Tratos Longos; Envolvimento
bilateral do trato corticoespinhal;
Um outro exame possível para o diagnóstico, é a análise
do DNA e exames pré-natais para pesquisa de mutações (Khandwala, et. al., 2004).
Estudos demostraram que “até 35% dos pacientes com uma insuficiência suprarrenal idiopática têm
elevados níveis de VLCFAs e podem, mais tarde, experimentar sintomas
neurológicos”. Daí, torna-se essencial medir os níveis de VLCFAs a todos
esses pacientes, sobretudo se são do sexo masculino, uma vez que esta simples
medição pode precocemente fazer o diagnóstico, permitindo uma intervenção e
retardar o aparecimento de outros sintomas (sintomas neurológicos) (Khandwala,
et. al., 2004).
Em suma, “a
medição dos níveis plasmáticos de VLCFAs constitui o teste de rastreio essencial
de escolha, seguida pela análise genética” (Khandwala, et. al., 2004).
TRATAMENTO
O tratamento de doentes com AMN é limitado e é dirigido
de acordo com a sintomatologia apresentada pelos pacientes. Assim existem três
grandes áreas de atuação (Khandwala, et. al., 2004):
· Terapia de Substituição Hormonal para a insuficiência suprarrenal
e/ou hipogonadismo que apresenta óptimos resultados;
· Instituição de uma dieta com baixo teor de gordura de forma a diminuir
as fontes exógenas de VLCFAs. Todavia, esta ao longo do tempo têm-se mostrado
ineficaz na retardo da evolução da doença. Assim, surgiu um novo tratamento que
resulta da administração de monoácidos graxos insaturados. Estes competem com
os saturados e como resultado diminuem os níveis de VLCFAs. Assim, a combinação
da restrição dietética e a administração do Óleo de Lorenzo, (trioleato de glicerilo) tem produzido
significativas reduções dos níveis plasmáticos de VLCFAs. O principal efeito
colateral deste óleo é a trombocitopenia que ocorre em 40% dos pacientes;
· Por fim, o único tratamento possível para reduzir os
sintomas neurológicos é o transplante de
medula óssea. Este deve ser realizado o mais precocemente possível,
idealmente nos estágios iniciais da doença.
BIBLIOGRAFIA
- · Fauci et al, Harrison – Medicina Interna, 17ª Edição;
- · ASSIES, J.; BARTH, P. G.; VAN GEEL, B. M.; WANDERS, R. J. A.; X (Fevereiro 1997), Linked Adrenoleukodystrophy: Clinical Presentation, Diagnosis, and Therapy. Journal of Neurology, Neurosurgery, and Psychiatry, 63:4-14
- KHANDWALA, H. M.; SPUREK, M.; VAN UUM, S.; GJEVRE, R. T. (Outubro 2004), Adrenomyeloneuropathy as a Cause of Primary Adrenal Insuffiency and Spastic Paraparesis. Canadian Medical Association or its Licensors, 171(9);
- KIM, J. H.; KIM, H. J. (Maio / Junho 2005), Childhood X-linked Adrenoleukodystrophy: Clinical-Pathologic Overview and MR Imaging Manifestations at Initial Evaluation and Follow-up. Radiographics, Vol 25 Nº3;







Sem comentários:
Enviar um comentário